富士胶片株式会社(以下简称“富士胶片”)和日本国立精神・神经医疗研究中心宣布了利用富士胶片全新的AI技术预测轻度认知功能障碍症(MCI)患者是否会在两年内进展为阿尔茨海默病(AD)的积极研究成果。这项用于AD进展预测的人工智能技术※1的准确率达88%※2,该研究成果已于4月12日在国际学术期刊《自然》杂志子刊《npj Digital Medicine》上发表※3。
该技术是由富士胶片基于其先进的图像识别技术以及机器学习方面的专业知识所开发的。
未来,富士胶片和日本国立精神・神经医疗研究中心将进一步验证该技术,以期更好地应用在针对AD疾病治疗的临床实验中,对患者进行分层。
主要研究成果
富士胶片利用其在摄影和医疗领域积累的先进图像识别技术,确立了以AI进行高精度预测的技术(AD进展预测AI技术),这项技术在可供研究数据有限的情况下,依然可以高精度地预测从MCI到AD的进展。所谓AD进展预测AI技术,是指以包括MRI图像、认知能力评分等信息在内的多种临床信息为基础的预测技术。
富士胶片和日本国立精神・神经医疗研究中心的一个研究小组※4,以不同人种(北美人和日本人)的患者数据库为对象,分别应用了AD进展预测AI技术,对MCI患者在2年内是否会发展为AD进行预测,结果表明预测准确率高达84-88%。由此证明,该项AD进展预测AI技术具有很高的可推广性。
研究背景与历程
据估计,目前全球约有5500万认知障碍症患者。而随着人口老龄化,预计到2050年这一数字将增加到约1.39亿。在认知障碍症中,AD患者(认知障碍症的一种)的人数最多,预计今后这一趋势还会继续。
近年来,在AD的新药研发过程中更倾向于以早期的MCI患者为对象实施临床试验,以观察β-淀粉样蛋白的存在情况,因为β-淀粉样蛋白是AD的主要致病物质,在发病前就已经开始蓄积。然而,大多数临床试验都没有成功,其中一个原因是,两年内从MCI进展到AD的患者比例不到20%※5,临床试验期间有很多MCI患者未发现有进展,被分配到对照组(服用安慰剂等)的患者也因未进展到AD而被认为其病情得到了控制。因此,从统计学角度而言无法得出可信结论。在这种情况下,富士胶片和日本国立精神・神经医疗研究中心认为,使用AI来预测哪些患者会从MCI发展到AD,并只对这些患者进行临床试验,能够正确地评估新药的有效性,使治疗与验证取得成功。
研究内容
近年来,大量研究报告表明,通过引入深度学习,图像识别准确率可以显着提升,但要达到深度学习的效果,需要大量的学习数据支持。然而,目前世界最大的AD研究项目NA-ADNI※6的公共数据库中,也不过只有约1000名MCI患者的数据。通常,在物体识别研究领域,要形成深度学习需要超过1000万张图像。在这种情况下,如何通过有限的数据确立高准确率的AI预测技术无疑是一项巨大的挑战。为了解决这个问题,富士胶片决定建立一种AD进展预测AI技术,以大脑中与AD进展高度相关的特定区域为对象,利用深度学习预测AD的进展。
技术确立
富士胶片利用其在摄影和医疗领域积累的先进图像识别技术,从脑部三维MRI图像中,分别对以①海马体、②前颞叶为中心的区域进行识别,因为,这两块区域被认为与AD进展最为相关。
利用深度学习,从以①海马体、②前颞叶为中心的两个区域,提取与AD进展相关的详细萎缩模式,并计算其图像特征※7。AI进而专注于两个区域确认的、对读片诊断起重要作用的海马体区域和杏仁体区域的萎缩模式,并依据其模式识别其向AD的进展(图1)。
使用NA-ADNI公共数据库的MCI患者数据进行学习。除了被认为与AD进展高度相关的脑内特定区域的图像特征外,还确立了通过认知能力测试评分等多种临床信息进行高精度AD进展预测的技术。
[图1]AI在预测AD进展中关注的详细萎缩模式(三维MRI检查图像)

全脑学习的AI(图1-A,A')不仅会关注与AD进展高度相关的海马体和杏仁体区域,而且还会关注与之不密切相关的脑脊髓液和枕叶。
另一方面,在以海马体(图1-B)或前颞叶(图1-C)为中心区域学习的AI,更加关注海马体或杏仁体区域的详细萎缩模式,在识别其是否会进展为AD方面比全脑学习的AI更加高效。
通过排除低相关性区域的学习,在有限的数据下深度学习减少了受到个体差异的影响,从而能获得较高的预测准确性。
技术验证
富士胶片和日本国立精神・神经医疗研究中心的研究小组,采用AD进展预测AI技术,预测2年内患者是否会从MCI进展至AD。除了将AD进展预测AI技术应用于NA-ADNI数据库外,还将其应用于未学习过的J-ADNI※8数据库,对该技术的预测准确性进行了客观的评估。
在预测MCI患者是否会发展为AD患者时,NA-ADNI的预测正确率为88%,J-ADNI为84%。
同时,与准确率同等重要的AI精度指标AUC※9,NA-ADNI为0.95、J-ADNI为0.91(图2)。
[图2]表示NA-ADNI和J-ADNI评估结果的ROC曲线※10
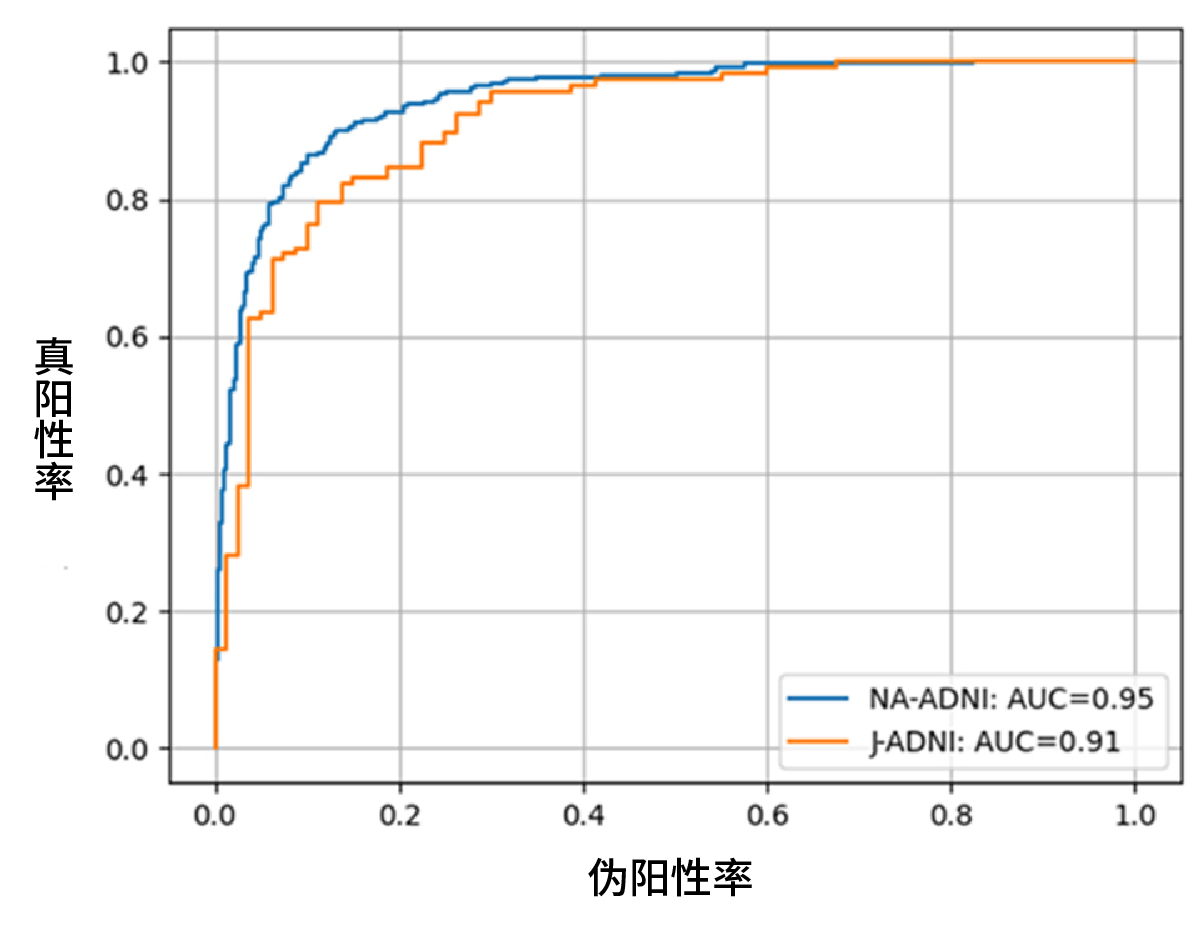
依据ROC曲线推导出的AUC(ROC曲线下的面积)指标,NA-ADNI为0.95、J-ADNI为0.91。AUC的最大值为1,表明在NA-ADNI和J-ADNI中都能高精度地预测AD进展。
综上所述,AD进展预测AI技术可以高精度地预测不同人种从MCI到AD的进展,属于可推广性较高的AI技术。
未来展望
富士胶片和日本国立精神・神经医疗研究中心将在临床试验数据中,对根据AD进展预测AI技术的预测结果分层的患者进行分析,以进一步验证这项技术的有效性。具体而言,通过AD进展预测AI技术预测患者的认知障碍症进展速度,并通过①对没有AD进展的患者不进行临床试验、②缩小对照组和治疗组之间在进展速度分布上的差异来研究提高临床试验成功率的可能性。力争在AD治疗药物的新临床试验中使用AD进展预测AI技术。
同时,还将探讨将AD进展预测AI技术的算法推广到各种精神疾病和神经系统疾病的脑部图像和临床数据中应用。这关系到患者预后和对治疗的反应预测,我们希望在推动个性化医疗方面能发挥重要作用。
本研究是在日本国立研究开发法人科学技术振兴机构产学共创平台共同研究推进项目(JST、OPERA、JPMJOP1842)的赞助下实施的。
※1 本技术不用于AD及其他疾病的诊断、治疗和预防。
※2 准确率是评价AI精度的指标之一,是描述预测结果与真实值相符程度的数值。
※3 发表的论文论文名:A high generalizability machine learning framework for predicting the progression of Alzheimer’s disease using limited data
作者:Caihua Wang, Yuanzhong Li, Yukihiro Tsuboshita, Takuya Sakurai, Tsubasa Goto, Hiroyuki Yamaguchi, Yuichi Yamashita, Atsushi Sekiguchi, Hisateru Tachimori and for Alzheimer’s Disease Neuroimaging Initiative
刊登杂志:npj Digital Medicine(国际学术期刊“自然”杂志的子刊)
URL:https://www.nature.com/articles/s41746-022-00577-x
doi:10.1038/s41746-022-00577-x
※4 神经研究所疾病研究第七部山口博行、山下祐一、精神保健研究所行动医学研究部关口敦、转化医疗中心(现为医院下属临床研究及教育研修部门 信息管理及解析部)立森久照
※5 Practice Guideline Update Summary: Mild Cognitive Impairment.(Petersen, R. C., et al. Neurology 16, 126-135 (2018))
※6 预测AD的发病、确认治疗药物疗效的研究项目,为全球最大。
ADNI是The Alzheimer’s disease neuroimaging initiative的缩写、主要由北美人组成的研究标为NA(North America)-ADNI。
※7 用数值化指示出参考图像的哪些部分才能发现进展预测的模式。
※8 日本厚生劳动省及NEDO等主导的AD研究项目。Japanese Alzheimer's Disease Neuroimaging Initiative的简称。
※9 表示AI判别精度的真阳性率与伪阳性率的指标。Area Under the Curve的缩写。真阳性率是指正确预测为阳性的数据的百分比,而伪阳性率是指将阴性数据错误预测为阳性的数据的百分比。AUC值为1意味着AI判断完全正确(真阳性率:100%,伪阳性率:0%)。如果真阳性率和伪阳性率相同,AUC值为0.5,则表示精度最低。
※10 表示一条曲线,其中计算了每个截止点的真阳性率和伪阳性率,绘制在一个平面上,真阳性率在纵轴上,伪阳性率在横轴上,并以直线连接。ROC是Receiver Operating Characteristic的缩写。ROC曲线下的面积为AUC的值。